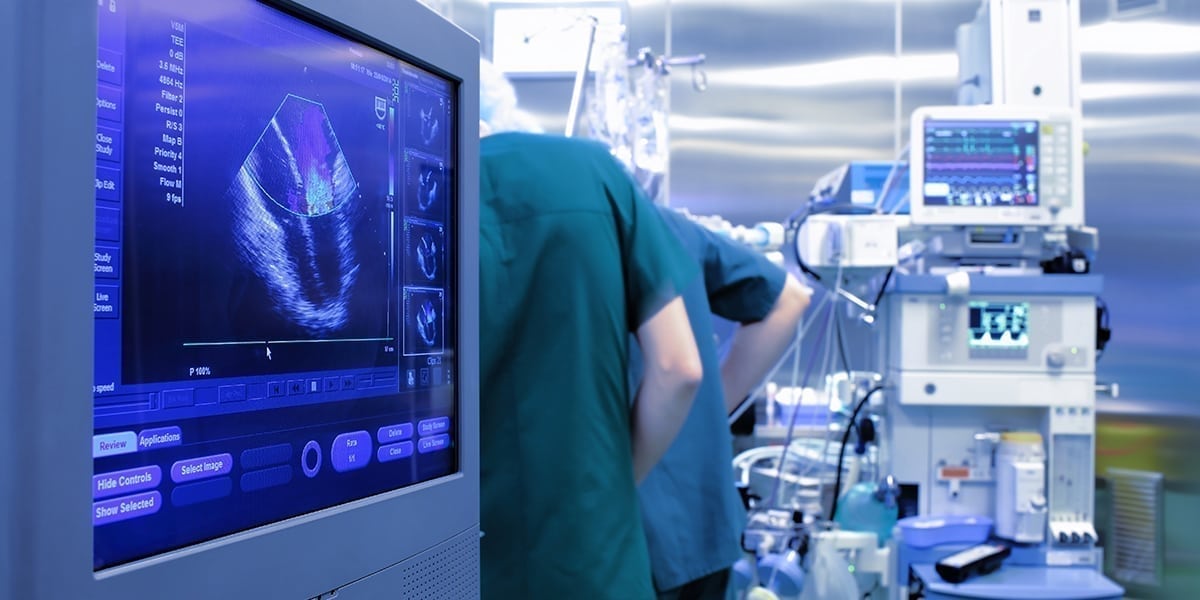
359 medizintechnische Geräte der Klassen II und III in China von klinischen Versuchen befreit.
Die NMPA (China Food and Drug Administration) veröffentlichte am 27.9.2016 mit Bekanntmachung 133, 2016 eine Liste von medizintechnischen Geräten der Klassen II und III, die bei der NMPA Registrierung keine klinischen Versuche mehr benötigen. Es handelt sich dabei um 267 Geräte der Klasse II und 92 Produkte der Klasse III. Insgesamt sind damit ab sofort in Klasse II 755 Geräte und in Klasse III 171 Geräte von den klinischen Versuchen in China befreit.
Umfangreichere Antragsdokumentation für NMPA Registrierung von medizintechnischen Geräten in China
Am 20.9.2016 veröffentlichte die NMPA die Bekanntmachung 178, 2016 von NMPA in der die Dokumentation von NMPA Anträgen neu geregelt wird. Nach der neuen Vorschrift muss der Antragsteller nicht, wie bisher üblich, nur einen Satz Originalantragsdokumente einreichen, sondern zusätzlich noch einen Satz Kopien und eine digitale Version der Anträge. Die neue Regelung tritt am 1.11.2016 in Kraft.
Weitere Informationen zu den angesprochenen Themen erhalten Sie bei:
Cisema GmbH
Tel.: +49 89 4161 7389 – 00
Fax: +49 89 7484 9956
info@cisema.de
www.cisema.de

 English
English  Italiano
Italiano  Français
Français  日本語
日本語  한국어
한국어