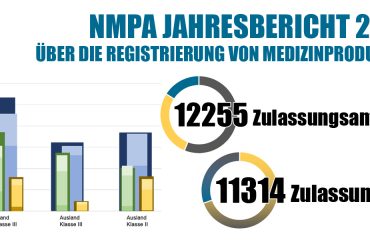
Am 10. Dezeber 2019 startete die NMPA (National Medical Products Administration) die Pilotphase der Online-UDID (Unique Device Identification Database) für Medizinproduktehersteller. Am 31.März 2020 wurde die UDID offiziell für die Öffentlichkeit freigegeben, so dass die Benutzer die Suchfunktion, das Herunterladen und die Datenaustauschfunktionen nutzen können.
Suchfunktion
Die Suchfunktion ist für Benutzer leicht zugänglich und ermöglicht eine schnelle Suche nach Produktnamen, Firmennamen oder UDI-Codes von Produkten in der Datenbank. Es bietet auch die erweiterte Suchfunktion zur Eingrenzung der Suchergebnisse bei komplexen Suchen. Nach Eingabe einer Suche nach einem bestimmten UDI-Code, Produktnamen oder Firmennamen steht eine Liste relevanter Informationen zum Herunterladen zur Verfügung.
Download
Die neuesten UDI-Informationen zu registrierten Medizinprodukten werden auf der Homepage der Website angezeigt und stehen in verschiedenen Batch-Formaten zum Herunterladen zur Verfügung: Alle, Monatlich, Wöchentlich, Täglich, usw., und bietet Informationen über das Erstellungsdatum, die Anzahl der Produkte und die Dateigröße.
Gemeinsame Nutzung von Daten
Verfügbar für NMPA-Rechtsvertreter, Wirtschaftsunternehmen oder medizinische Einrichtungen, die sich über die API-Schnittstelle für den Datenaustausch verbinden können.
Welche Auswirkungen hat die UDID auf die Kennzeichnung und Verpackung von Medizinprodukten?
Der UDI-Code muss für Produkte aufgebracht werden, die am oder ab dem 1. Oktober 2020 hergestellt werden.
Wer ist für die Übermittlung von UDI-Daten an die NMPA verantwortlich?
Der NMPA-Rechtsvertreter, der von den Antragstellern im Ausland ernannt wird, ist für die Beantragung und Einreichung von UDI-Daten verantwortlich.
Weitere Informationen über die UDI-Anforderungen für Medizinprodukte in China finden Sie hier.
Von Jacky Li. Wenden Sie sich an Cisema, um mehr zu erfahren.

 English
English  Italiano
Italiano  Français
Français  日本語
日本語  한국어
한국어