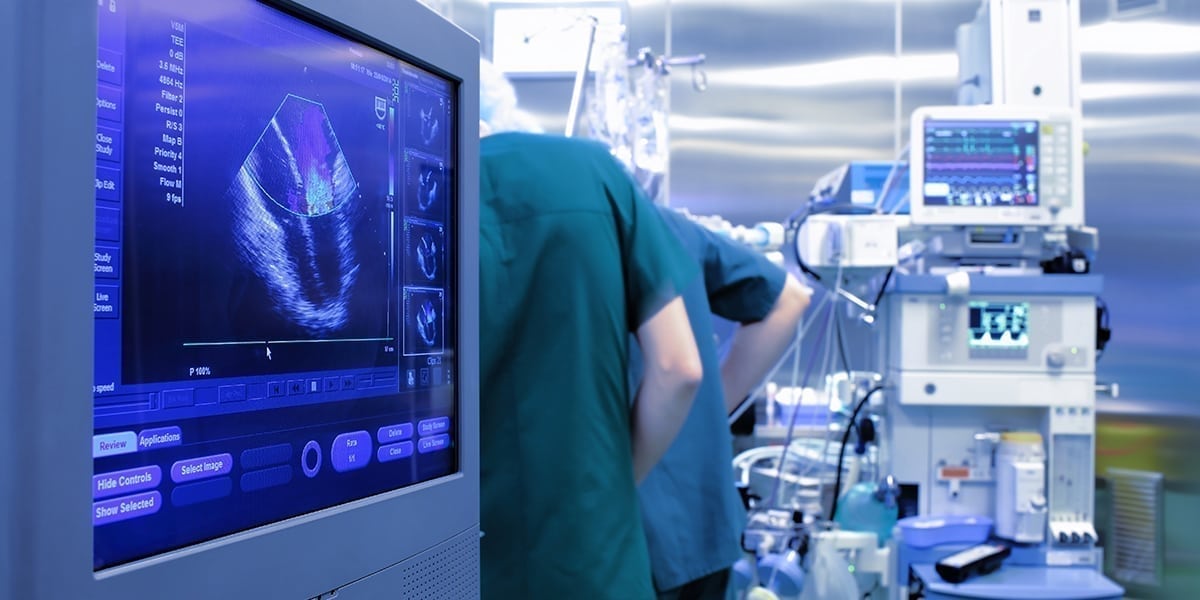
Am 05.11.2018 veröffentlichte die NMPA (früher NMPA) das “Special Approval Procedures for Innovative Medical Devices” (NMPA Nr. 83-2018), welches am 1. Dezember 2018 in Kraft treten wird. Der Entwurf (NMPA Nr. 13-2014) wurde aufgehoben. Das Dokument erläutert die Überprüfung und Anforderungen für innovative Medizinprodukte.
- Leistungen
- NMPA Registrierung – Medizinprodukte und IVD
- DMF (Drug Master Filing) – Pharmazeutische Produkte
- NMPA Registrierung – Kosmetika
- NMPA Registrierung – Funktionelle Lebensmittel
- CML (China Manufacture Licence) – Druckbehälter
- CCC (China Compulsory Certification) – Industrie- und Konsumgüter
- Weiteres/Sonstiges
- Über uns
- Veranstaltungen
- MEDIEN & RESSOURCEN

 English
English  Italiano
Italiano  Français
Français  日本語
日本語  한국어
한국어