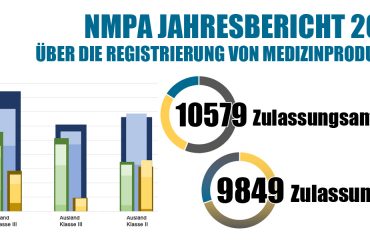
Am 12.07.2019 veröffentlichte die NMPA einen Entwurf für die Prüfungsanforderungen von Medizinprodukt-Zulassungsanträgen (Nr. 42-2019). Die CMDE der NMPA ist nun zusätzlich im Zulassungsprozess eingebunden, indem sie die Vollständigkeit, Konformität und Konsistenz von Antragsunterlagen gemäß den neuesten Anforderungen überprüft.
- Leistungen
- NMPA Registrierung – Medizinprodukte und IVD
- DMF (Drug Master Filing) – Pharmazeutische Produkte
- NMPA Registrierung – Kosmetika
- NMPA Registrierung – Funktionelle Lebensmittel
- CML (China Manufacture Licence) – Druckbehälter
- CCC (China Compulsory Certification) – Industrie- und Konsumgüter
- Weiteres/Sonstiges
- Über uns
- Veranstaltungen
- MEDIEN & RESSOURCEN

 English
English  Italiano
Italiano  Français
Français  日本語
日本語  한국어
한국어