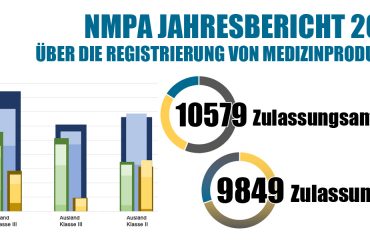
Am 24. Dezember veröffentlichte das Zentrum für die Normung von Medizinprodukten der NMPA (National Medical Products Administration) den zweiten Entwurf des Klassifizierungskatalogs für Medizinprodukte, um die Öffentlichkeit um Kommentare zu bitten. In dem Entwurf wird vorgeschlagen, sieben Produktkategorien von Klasse III in Klasse II herabzustufen, während unsterile flüssige und pastöse Verbänd als Medizinprodukte der Klasse II statt der Klasse I eingestuft werden sollen.
Am 31. Dezember 2021 veröffentlichte die NMPA (Nr.158 – 2021) den neuen Produktkatalog für Medizinprodukte der Klasse I. Der neue Katalog umfasst 19 Unterverzeichnisse der vorherigen Version von 2017 und besteht aus 119 primären Produktkategorien, 368 sekundären Produktkategorien und 2629 Beispielen von Produktnamen. Gegenüber der Vorgängerversion wurden 90 Produktinformationen und 538 Beispiele für Produktnamen hinzugefügt. Der neue Katalog trat am 1. Januar 2022 in Kraft.
Für Produkte, die vor dem 1. Januar 2022 angemeldet wurden und noch als Medizinprodukte der Klasse I gemäß dem neuen Klasse-I-Katalog geführt werden, muss der Anmelder die Änderung der Anmeldeinformationen vor dem 1. April 2022 vornehmen, wenn die im Formular für die Anmeldeinformationen veröffentlichten Inhalte und die relevanten Inhalte der PTR für die Anmeldung nicht mit dem neuen Klasse-I-Katalog übereinstimmen. Andernfalls kann der Antragsteller bei der ursprünglich anmeldenden Stelle die Löschung der ursprünglichen Anmeldung beantragen und die Anmeldung von Medizinprodukten der Klasse I erneut einreichen. IVD-Testreagenzien und Kombinationsprodukte sind in dem neuen Katalog nicht enthalten.
Highlights
- Geräte für die Kühltherapie, Zubehör für Lichttherapiegeräte, Pflaster, Akupressurgeräte usw., die der Risikoklasse I angehören, dürfen keine Bestandteile wie chinesische Arzneimittel, pharmazeutische Chemikalien, biologische Produkte usw. mehr enthalten.
- Bisher konnten flüssige und pastöse Verbände je nach Verwendungszweck odr Anwendungsmethode in die Klassen I, II und III eingeteilt werden; nicht sterile flüssige und pastöse Verbände werden jedoch nicht mehr als Medizinprodukte der Klasse I eingestuft, da sie aus dem neuen Katalog für Medizinprodukte der Klasse I gestrichen wurden. Der Vorschlag der NMPA für den neuen Klassifizierungskatalog für Medizinprodukte (Entwurf) steht im Einklang mit dieser Änderung.
Die Klassifizierung von Medizinprodukten ist die Grundlage für das Risikomanagement von Medizinprodukten und ein wichtiger Bestandteil der Reform des chinesischen Prüfungs- und Zulassungssystems für Medizinprodukte. Wenn Sie mehr über die Änderungen der Klassifizierungsvorschriften für Ihre Produkte in China wissen möchten, wenden Sie sich bitte an Cisema, wir helfen Ihnen gerne bei der Evaluierung.
By Alice Liu and Jacky Li.

 English
English  Italiano
Italiano  Français
Français  日本語
日本語  한국어
한국어