Am 18.März 2020 veröffentlichte die NMPA (National Medical Products Administration) ihren Jahresbericht 2019 über die Registrierung von Medizinprodukten.
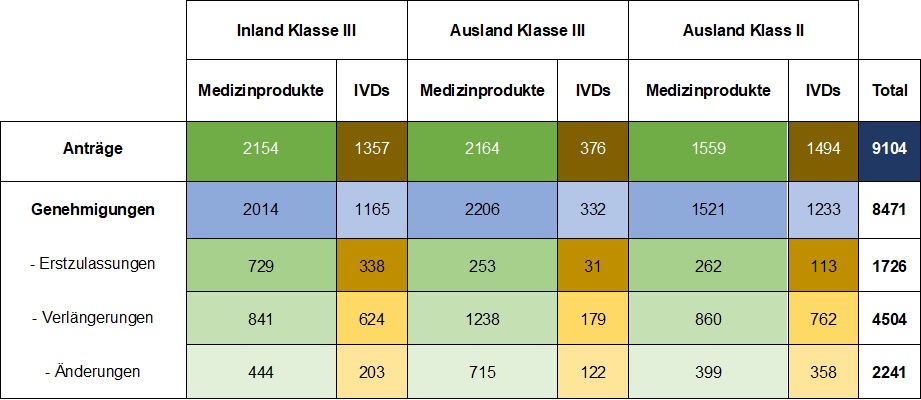
Im Jahr 2019 gingen bei der NMPA insgesamt 9.104 Anträge für die Erstzulassung, Zulassungsverlängerungen und Änderungen in der Zulassung von Medizinprodukten der Klasse III (In- und Ausland) und der Klasse II (Ausland) ein, was einem Anstieg von 37,8% gegenüber 2018 entspricht. Von den 9.104 Anträgen genehmigte das NMPA insgesamt 8.471 Anträge, was einem Anstieg von 53,2% gegenüber 2018 entspricht. Außerdem bearbeitete das NMPA insgesamt 1.383 Anträge für importierte Medizinprodukte der Klasse I, was einem Rückgang von 20,7% gegenüber 2018 entspricht.
Tabelle 1: Anzahl der Anträge und Zulassungen für Medizinprodukte und IVDs bei der NMPA
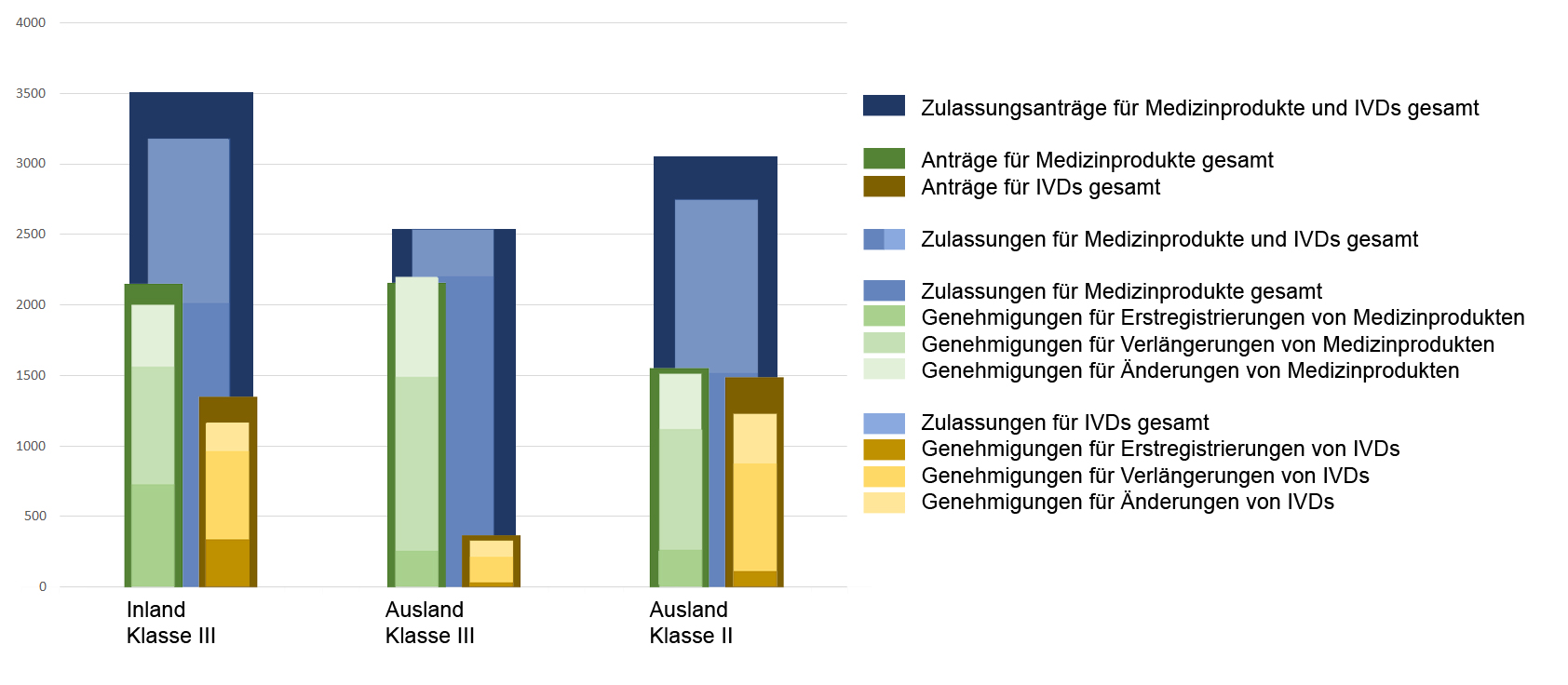
Grafik 1: Anzahl der Anträge und Zulassungen für Medizinprodukte und IVDs bei der NMPA
Grafik 2: Prozentuale Verteilung der drei Zulassungsarten bei der NMPA

Grafik 3: Prozentuale Aufteilung der Zulassungen von Medizinprodukten und IVDs bei der NMPA

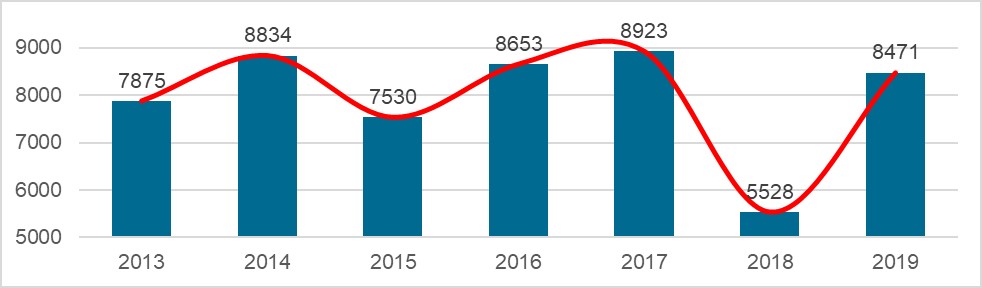
Grafik 4: Anzahl der genehmigten Neuregistrierungen von Januar 2013 bis Dezember 2019 bei der NMPA
Grafik 5: Anzahl der genehmigten Neuregistrierungen von Januar 2019 bis Dezember 2019 bei der NMPA
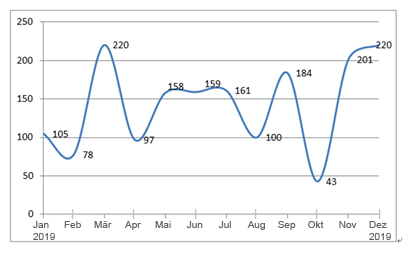
Im Jahr 2019 genehmigte die NMPA insgesamt 1.726 Neuregistrierungen.
Die Genehmigungsbehörden für Medizinprodukte in den Provinzen (MPAs) genehmigten insgesamt 17.017 Anträge für inländische Medizinprodukte der Klasse II in China, was einem Anstieg von 53,4% gegenüber 2018 entspricht.
Die Genehmigungsbehörden für Medizinprodukte in den Städten (MPAs) bearbeiteten insgesamt 16.754 Anträge auf die Zulassung von inländischen Medizinprodukten der Klasse I in China, was einem Rückgang von 2,4% gegenüber 2018 entspricht.
China konzentriert sich weiterhin auf den Import von hochwertigen und teuren medizinischen Geräten aus dem Ausland. Die fünf wichtigsten Produktgruppen der Klasse II und III ausländischer Herkunft, die 2019 registriert werden sollten, waren:
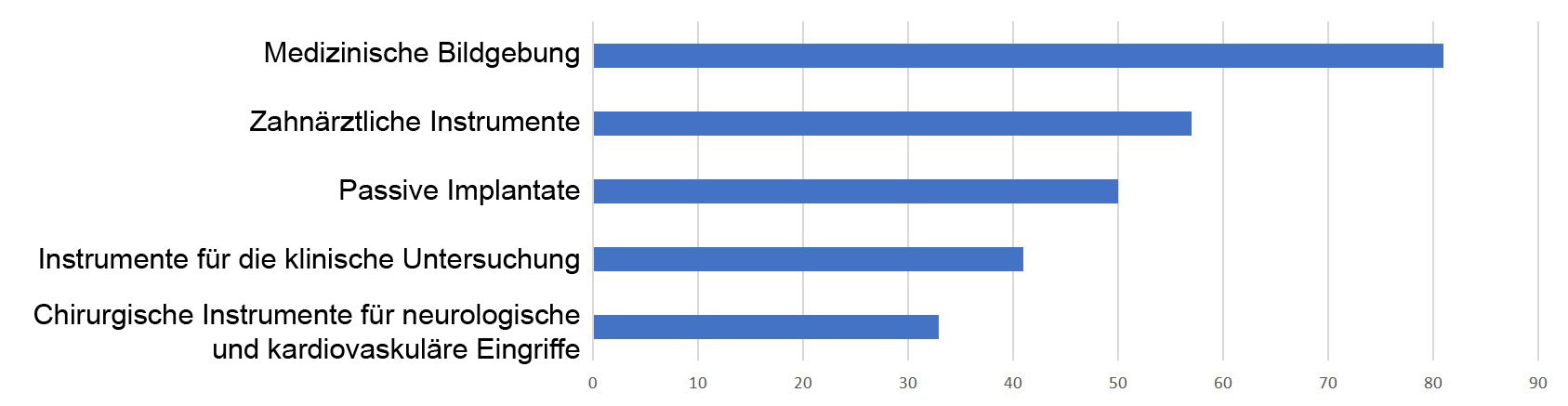
1. Medizinische Bildgebung (81 Registrierungen)
2. Zahnärztliche Instrumente (57 Anmeldungen)
3. Passive Implantate (50 Registrierungen)
4. Instrumente für die klinische Untersuchung (41 Anmeldungen)
5. Chirurgische Instrumente für neurologische und kardiovaskuläre Eingriffe (33 Anmeldungen)
Grafik 6: Die Top 5 – Registrierung von ausländischen Medizinprodukten der Klasse II und III im Jahr 2019
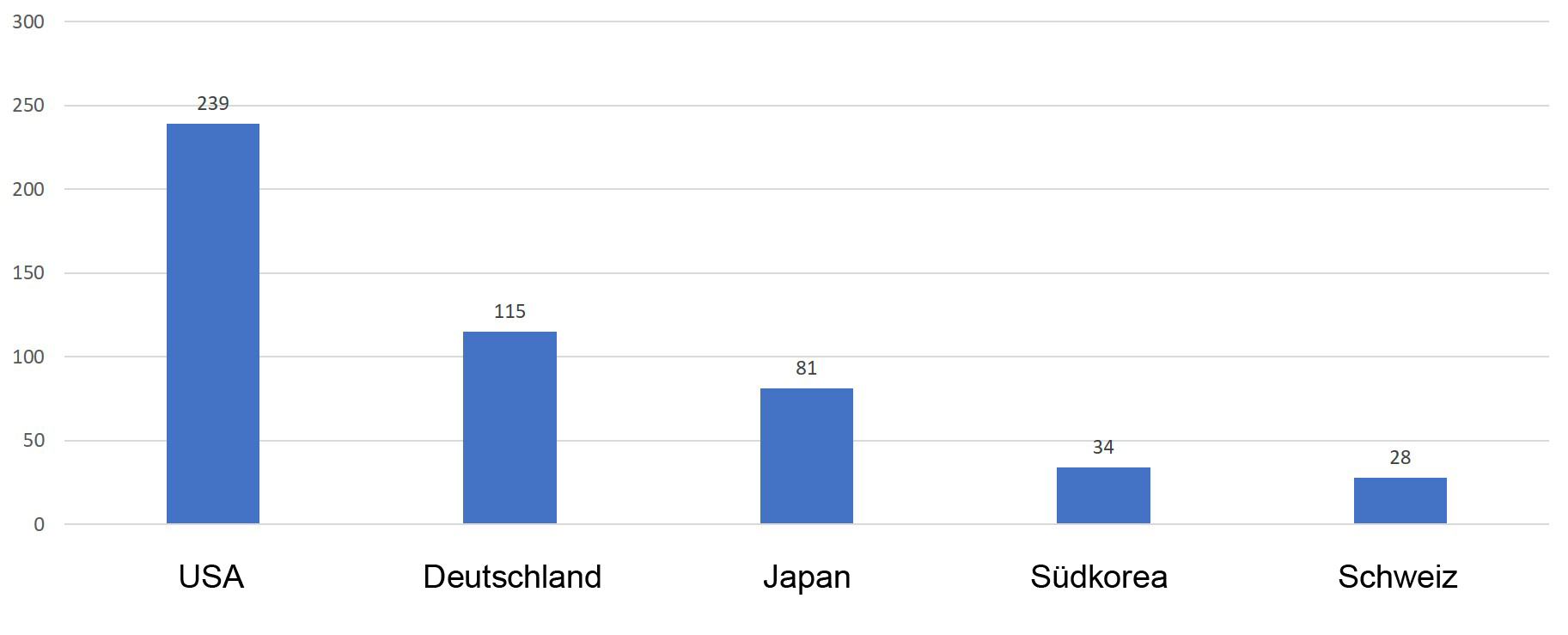
Die Vereinigten Staaten von Amerika, Deutschland, Japan, Korea und die Schweiz haben die höchste Anzahl von Erstzulassungen für medizinische Geräte in China, die bis zu 75,4% der gesamten Erstzulassungen für medizinische Geräte ausmachen.
Grafik 7: Die Top 5 Länder – Export von Medizinprodukten im Jahr 2019 nach China
Besondere Zulassungsverfahren für innovative Medizinprodukte
Die NMPA erhielt insgesamt 179 Anträge auf Sonderprüfung und Zulassung innovativer medizinischer Geräte, darunter 31 Anträge auf vorrangige Prüfung. Insgesamt wurden 19 innovative medizinische Geräte genehmigt:
Ausland
1) Micra TPS, sondenloses Transkatheter-Schrittmachersystem
Inland
2) PET/CT-Bildgebungssystem
3) Nukleinsäure-Amplifikations-Nachweisanalysator
4) Dezellularisiertes Hornhaut-Implantat
5) Linksatriales Anhängsel-Okkluder-System
6) Stentgraft und Einführsystem für die Bauchaorta
7) Bioresorbierbares Koronar-Rapamycin-eluierendes Stentsystem
8) Poröses Knochen-Füllmaterial aus Tantal
9) Patientenmonitor
10) Verschluss des linken Vorhofanhangs
11) Software für ein intensitätsmoduliertes Strahlentherapie-Planungssystem
12) Digitales Mammographie-System
13) Transkatheter-Aortenklappensystem
14) Intravaskulärer Einweg-Bildgebungskatheter
15) Nicht-invasives Blutzuckermessgerät
16) Implantierbares linksventrikuläres Assistenzsystem
17) Koronarangiographisches Blutfluss-Reservefraktionsmesssystem
18) Invasiver Einweg-Drucksensor
19) Positronenemissions- und Röntgen-Computertomographie-Scansystem PET/CT
Weitere Informationen zu diesem Thema erhalten Sie bei
Cisema (Hong Kong) Limited
Tel.: +852 3462 2483
info@cisema.com
www.cisema.com/en

 English
English  Italiano
Italiano  Français
Français  日本語
日本語  한국어
한국어